|
|
MODULE 3 Vibration-rotation
des molécules diatomiques
Problèmes
-
Le spectre de rotation-vibration de
l'oxyde de carbone comporte dans le proche infrarouge une
bande intense dans la région de
2100-2200 cm–1. Avec un appareil de
basse résolution on obtient la série de
raies suivantes : 2124, 2128, 2132, 2136, 2140,
2148, 2152, 2156, 2160 cm–1.
- Déterminez le moment d'inertie, la
distance internucléaire et la fréquence
de vibration de la molécule CO.
- Déterminez la valeur de la constante de
distorsion centrifuge de la même
molécule.
Corrigé
-
La fréquence fondamentale de
l'élongation O-H dans le méthanol est
située à 3300 cm–1.
Prédisez la position de la bande correspondante
pour l'espèce isotopique CH3OD.
Note : Il n'y a pas de corrigés
pour ce problème, ainsi que pour les
problèmes 3 à 5.
- Le spectre infrarouge de H35Cl sous haute
résolution montre des raies d'absorption dont les
fréquences sont indiquées dans le tableau
qui suit. En utilisant un logiciel (ordinateur,
micro-ordinateur ou calculatrice appropriée),
calculez au moyen d'une régression linéaire
ou d'un moindre carré les coefficients du
polynôme suivant :
E = b + am + cm2 + dm3,
où E est l'énergie de la raie et
m un nombre entier.
Établissez au préalable la
valeur de m pour chaque raie (colonne 3 du tableau
suivant). Déduisez-en :
- l'énergie de la raie manquante;
- la valeur de ωe – 2
ωexe;
- les constantes B (υ = 0) et
B′ (υ = 1);
- la constante de distorsion centrifuge
D.
Tracez les courbes E (cm–1)
= f (J) et E (cm–1)
= f (m) sur le même graphe.
Spectre de
rotation-vibration de H35Cl.
|
J
|
Énergie (cm–1)
|
m
|
ΔE (cm–1)
|
Δ(ΔE) (cm–1)
|
|
|
10
|
3072,8558
|
|
|
|
|
|
|
|
|
13,5338
|
|
|
|
9
|
3059,3220
|
|
|
-0,7244
|
|
|
|
|
|
14,2582
|
|
|
|
8
|
3045,0638
|
|
|
-0,7132
|
|
|
|
|
|
14,9714
|
|
|
|
7
|
3030,0924
|
|
|
-0,7036
|
|
|
|
|
|
15,6750
|
|
|
|
6
|
3014,4174
|
|
|
-0,6971
|
|
|
|
|
|
16,3721
|
|
|
|
5
|
2998,0453
|
|
|
-0,6598
|
|
|
|
|
|
17,0319
|
|
|
|
4
|
2981,0134
|
|
|
-0,6912
|
|
|
|
|
|
17,7231
|
|
|
|
3
|
2963,2903
|
|
|
-0,6461
|
|
|
|
|
|
18,3692
|
|
|
|
2
|
2944,9211
|
|
|
-0,6493
|
|
|
|
|
|
19,0185
|
|
|
|
1
|
2925,9026
|
|
|
-0,6300
|
|
|
|
|
|
19,6485
|
|
|
|
0
|
2906,2541
|
|
|
--
|
|
|
-
|
|
|
|
|
|
|
1
|
2865,1047
|
|
|
|
|
|
|
|
|
21,4745
|
|
|
|
2
|
2843,6302
|
|
|
-0,5816
|
|
|
|
|
|
22,0561
|
|
|
|
3
|
2821,5741
|
|
|
-0,5694
|
|
|
|
|
|
22,6255
|
|
|
|
4
|
2798,9486
|
|
|
-0,5565
|
|
|
|
|
|
23,1880
|
|
|
|
5
|
2775,7666
|
|
|
-0,5445
|
|
|
|
|
|
23,7265
|
|
|
|
6
|
2752,0401
|
|
|
-0,5288
|
|
|
|
|
|
24,2553
|
|
|
|
7
|
2727,7848
|
|
|
-0,5170
|
|
|
|
|
|
24,7723
|
|
|
|
8
|
2703,0125
|
|
|
-0,5041
|
|
|
|
|
|
25,2764
|
|
|
|
9
|
2677,7361
|
|
|
|
|
|
Données
aimablement transmises par le prof. R. Colin,
chimie-physique moléculaire
Université Libre de Bruxelles,
Bruxelles.
|
- Répétez le même problème
pour HBr, à partir de la liste suivante des
énergies des raies (en cm–1).
|
2 371,71
|
2 471,13
|
2 575,52
|
2 650,08
|
|
2 392,50
|
2 489,66
|
2 591,33
|
2 663,63
|
|
2 412,83
|
2 507,73
|
2 606,70
|
2 676,74
|
|
2 432,72
|
2 525,36
|
2 621,61
|
2 689,39
|
|
2 452,15
|
2 542,53
|
2 636,07
|
2 701,59
|
- Répétez le même problème
pour H37Cl.
|
2 675,9584
|
2 796,9750
|
2 923,7377
|
3 012,1328
|
|
2 701,1927
|
2 819,5661
|
2 942,7279
|
3 027,7879
|
|
2 725,9250
|
2 841,5877
|
2 961,0732
|
3 042,7419
|
|
2 750,1418
|
2 863,0289
|
2 978,7650
|
3 056,9840
|
|
2 773,8293
|
2 904,1162
|
2 995,7878
|
3 070,5036
|
- Le spectre infrarouge de DCl sous haute
résolution montre des raies d'absorption dont les
fréquences sont indiquées dans le tableau
ci-dessous. En vous servant des intensités
mesurées des raies, départagez les raies
appartenant à D35Cl et celles
appartenant à D37Cl. En vous inspirant
du problème 3 relatif à
H35Cl, calculez au moyen d'une
régression linéaire ou d'un moindre
carré, et cela pour chacune des deux
molécules isotopiques, les coefficients du
polynôme suivant :
E = b + am + cm2 + dm3,
où E est l'énergie de la raie et
m un nombre entier.
Établissez au préalable les
valeurs de J et m pour chaque raie.
Déduisez-en, pour D35Cl et
D37Cl :
- l'énergie de la raie manquante;
- la valeur de ωe – 2
ωexe;
- les constantes B (υ = 0) et
B′ (υ = 1), ainsi que
les longueurs de liaison correspondantes;
- la constante de distorsion centrifuge
D.
Tracez les courbes E (cm–1)
= f (J) et E (cm–1)
= f (m) sur le même graphe.
Corrigé
Spectre de
rotation-vibration de DCl : raies observées (υ
= 0 → υ = 1).
|
nº
|
Énergie
(cm–1)
|
Absorbance
|
nº
|
Énergie
(cm–1)
|
Absorbance
|
|
1
|
2230,8479
|
0,043
|
31
|
2080,2753
|
1,096
|
|
2
|
2224,0387
|
0,089
|
32
|
2077,3076
|
0,384
|
|
3
|
2216,9606
|
0,156
|
33
|
2069,2694
|
1,761
|
|
4
|
2213,6323
|
0,049
|
34
|
2066,3342
|
0,686
|
|
5
|
2209,6132
|
0,280
|
35
|
2058,0468
|
2,133
|
|
6
|
2206,3007
|
0,086
|
36
|
2055,1451
|
0,866
|
|
7
|
2202,0025
|
0,455
|
37
|
2046,6072
|
2,224
|
|
8
|
2198,7071
|
0,156
|
38
|
2043,7399
|
0,888
|
|
9
|
2194,1272
|
0,696
|
39
|
2034,9590
|
2,186
|
|
10
|
2190,8502
|
0,243
|
40
|
2032,1271
|
0,875
|
|
11
|
2185,9952
|
0,997
|
41
|
2023,1001
|
1,998
|
|
12
|
2182,7377
|
0,346
|
42
|
2020,3044
|
0,764
|
|
13
|
2177,6036
|
1,360
|
43
|
2011,0405
|
1,761
|
|
14
|
2174,3672
|
0,487
|
44
|
2008,2814
|
0,654
|
|
15
|
2168,9620
|
1,709
|
45
|
1998,7764
|
1,436
|
|
16
|
2165,7472
|
0,638
|
46
|
1996,0555
|
0,521
|
|
17
|
2160,0666
|
2,006
|
47
|
1986,3186
|
1,105
|
|
18
|
2156,8750
|
0,783
|
48
|
1983,6365
|
0,381
|
|
19
|
2150,9268
|
2,201
|
49
|
1973,6637
|
0,785
|
|
20
|
2147,7596
|
0,901
|
50
|
1971,0211
|
0,263
|
|
21
|
2141,5397
|
2,336
|
51
|
1960,8216
|
0,533
|
|
22
|
2138,3978
|
0,984
|
52
|
1958,2191
|
0,173
|
|
23
|
2131,9144
|
2,342
|
53
|
1947,7905
|
0,344
|
|
24
|
2128,7986
|
1,000
|
54
|
1945,2297
|
0,112
|
|
25
|
2122,0484
|
2,221
|
55
|
1934,5784
|
0,198
|
|
26
|
2118,9605
|
0,918
|
56
|
1932,0590
|
0,067
|
|
27
|
2111,9499
|
1,845
|
57
|
1921,1853
|
0,111
|
|
28
|
2108,8904
|
0,713
|
58
|
1918,7094
|
0,036
|
|
29
|
2101,6186
|
1,138
|
59
|
1907,6167
|
0,058
|
|
30
|
2098,5888
|
0,392
|
60
|
1893,8780
|
0,031
|
|
Données
aimablement transmises par le prof. R. Colin,
chimie-physique moléculaire
Université Libre de Bruxelles,
Bruxelles.
|
- Mêmes questions pour la transition (υ
= 0 → υ = 2). Corrigé
Spectre de
rotation-vibration de DCl : raies observées (υ
= 0 → υ = 2).
|
nº
|
Énergie
(cm–1)
|
Absorbance
|
nº
|
Énergie
(cm–1)
|
Absorbance
|
|
1
|
4226,6804
|
0,056
|
23
|
4132,8950
|
0,047
|
|
2
|
4221,9699
|
0,064
|
24
|
4117,6476
|
0,136
|
|
3
|
4216,7621
|
0,109
|
25
|
4111,8404
|
0,049
|
|
4
|
4211,0878
|
0,162
|
26
|
4106,4180
|
0,245
|
|
5
|
4210,7603
|
0,052
|
27
|
4100,6380
|
0,075
|
|
6
|
4204,9374
|
0,250
|
28
|
4094,7565
|
0,295
|
|
7
|
4198,8805
|
0,091
|
29
|
4089,0130
|
0,104
|
|
8
|
4198,2980
|
0,270
|
30
|
4082,6384
|
0,306
|
|
9
|
4192,2631
|
0,093
|
31
|
4076,9159
|
0,095
|
|
10
|
4191,1839
|
0,331
|
32
|
4070,1033
|
0,287
|
|
11
|
4185,1716
|
0,103
|
33
|
4064,4441
|
0,089
|
|
12
|
4183,6147
|
0,357
|
34
|
4057,1180
|
0,249
|
|
13
|
4177,6210
|
0,1222
|
35
|
4051,4871
|
0,080
|
|
14
|
4175,5631
|
0,395
|
36
|
4043,7218
|
0,203
|
|
15
|
4169,5941
|
0,123
|
37
|
4038,1402
|
0,072
|
|
16
|
4167,0576
|
0,399
|
38
|
4029,8939
|
0,170
|
|
17
|
4161,1125
|
0,128
|
39
|
4024,3623
|
0,061
|
|
18
|
4158,0845
|
0,352
|
40
|
4015,6564
|
0,121
|
|
19
|
4152,1627
|
0,122
|
41
|
4010,1606
|
0,041
|
|
20
|
4148,6556
|
0,279
|
42
|
4000,9944
|
0,087
|
|
21
|
4142,7492
|
0,092
|
43
|
3985,9164
|
0,061
|
|
22
|
4138,7699
|
0,145
|
44
|
3970,4534
|
0,042
|
|
Données
aimablement transmises par M. Carleer du
laboratoire du prof. R. Colin, chimie-physique
moléculaire, Université Libre de
Bruxelles, Bruxelles.
|
- Pour la molécule DCl, la documentation donne
les informations numériques suivantes (en cm–1)
:
Be = 5,448
794, αe = 0,113
291
En utilisant la relation qui existe entre
la constante de rotation et le niveau de vibration,
comparez les valeurs obtenues pour les valeurs de
B (υ = 0),
B (υ = 1) et
B (υ = 2) des deux
problèmes précédents. Corrigé
- Vérifiez graphiquement que B varie
comme l'inverse de la distance internucléaire dans
le cas de divers états électroniques de
l'oxyde de carbone. Déterminez de la même
manière, en traçant les graphes
appropriés, la dépendance de ωe
avec la distance internucléaire.
Que pouvez-vous dire de la relation, s'il en existe une,
entre ωe et la distance
internucléaire? Corrigé
|
État électronique
|
re
(pm)
|
B
(cm–1)
|
ωe
(cm–1)
|
|
X 1Σ+
|
112,83
|
1,9313
|
2169,8
|
|
a 3Πr
|
120,57
|
1,6912
|
1743,4
|
|
a′ 3Σ+
|
135,23
|
1,3446
|
1228,6
|
|
d 3Δi
|
136,96
|
1,3109
|
1171,9
|
|
e 3Σ–
|
138,4
|
1,2836
|
1117,7
|
|
A 1Π
|
123,53
|
1,6115
|
1518,2
|
|
I 1Σ–
|
139,11
|
1,2705
|
1092,2
|
|
D 1Δ
|
139,9
|
1,257
|
1094,0
|
|
b 3Σ+
|
111,3
|
1,986
|
2199,3
|
|
Valeurs tirées
de http://webbook.nist.gov/chemistry/name-ser.html
|
- Pour la molécule C=S, on observe les valeurs
suivantes (en cm–1) : ωe = 1285,08,
Be = 0,8200 et
De = 1,43 × 10–6.
Comparez la valeur de ωe obtenue
à l’aide de l’approximation 3.6
avec la valeur expérimentale. Corrigé
Problèmes avec VR
Molécules
- Placez VR Molécules à la page 6.
En faisant varier si nécessaire les nombres
quantiques, déterminez les valeurs des constantes
ωe, ωexe,
Be et αe
pour la molécule HCl. Corrigé
- Placez VR Molécules à la page 7.
Vérifiez les relations 3.7, 3.8 et 3.9 pour ces
deux variantes de la molécule d'hydrogène.
Corrigé
- Placez VR Molécules à la page 8.
En cliquant sur le nom de la molécule
contrôlée, en haut à gauche,
sélectionnez une des molécules
suivantes : O2, Cl2, HF, CO,
N2. Pour la molécule que vous avez
choisie, déterminez le plus grand nombre de
constantes moléculaires possible. N'oubliez pas
d'activer si nécessaire les corrections
d'énergie (dans la fenêtre en bas à
gauche portant ce nom, qui apparaît ou
disparaît quand on clique sur le bouton ΔE
situé sous le nom de la molécule.)
Corrigé
Corrigés
-
- On note que les raies sont
également espacées d’une
énergie de 4 cm–1.
2B = 4
cm–1 et
B = 2 cm–1
On reconnaît sans
difficulté l’absence d’une raie
à 2144 cm–1. Cette raie
représente la transition de vibration pure.
Cette transition est inexistante à cause de la
règle de sélection ΔJ = ±1.
Les raies situées à des énergies
supérieures font partie des raies riches,
R (ΔJ = +1) et celles
à plus basses énergies sont
appelées les raies pauvres, P (ΔJ = –1).
Le moment d’inertie de la
molécule est obtenu à l’aide de la
relation :
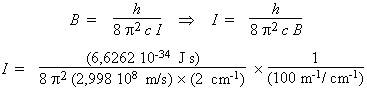
I =
14,00 × 10–47 kg
× m2
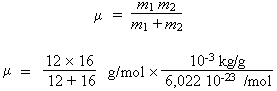
μ =
1,1387 10–26 kg
Le facteur 10–3 est
introduit pour tenir compte du fait que les masses
atomiques sont exprimées en kg/mol et que le
rotateur étant bien la molécule, la
masse de la molécule est égale à
la masse molaire divisée par le nombre
d’Avogadro.
En remplaçant chaque valeur
littérale par sa valeur numérique, on
obtient :
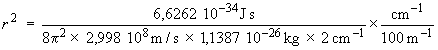
r2
= 1,229 × 10–20
m2
⇒
r = 1,109 × 10–10
m = 110,9 pm
Notons que ce résultat peut
être obtenu plus simplement grâce à
la relation
r2 = I / μ.
- Les données numériques
suggèrent que l'intervalle entre les raies est
constant, ce qui laisse entrevoir que la constante de
distorsion centrifuge est nulle, ou du moins
très faible. Pour obtenir sa valeur, il aurait
fallu utiliser un appareil de mesure à grande
résolution, de façon à pouvoir
mesurer les raies avec une précision de un ou
deux ordres de grandeur supérieure. Par
ailleurs, l’observation et la mesure de plusieurs
autres raies auraient sans doute facilité cette
mesure.
-
Calcul de l'énergie de la raie
manquante.
Une méthode simple, utile mais non
rigoureuse, consiste à réaliser que la
valeur de la raie manquante peut se déduire
approximativement de la moyenne arithmétique de la
valeur des deux raies qui encadrent cette raie.
Énergie (raie
manquante) = [ E(J = 0 → J = 1)
+ E(J = 1 → J = 0)
] / 2
En portant sur un graphe
l'intensité de la raie en fonction de son
énergie exprimée en cm–1
(figure ci-dessous), on observe que l'on a deux groupes
de raies.
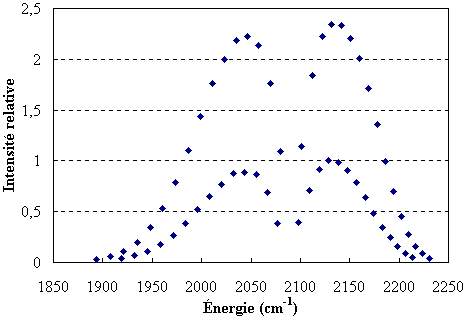
Compte tenu des proportions isotopiques, la
série de raies plus intenses correspond au
D35Cl et l'autre au D37Cl. On peut
donc constituer un tableau (voir tableau suivant) dans
lequel on a regroupé dans les deux
premières colonnes ce qui a trait au
D35Cl et dans les 5e et
6e colonnes ce qui correspond au
D37Cl. Dans le premier cas, la raie manquante
aurait une énergie telle que :
Énergie (raie
manquante) = [ 2 101,62 + 2 080,27 ] / 2 = 2
090,94 cm–1
De la même manière, pour
D37Cl :
Énergie (raie
manquante) = [ 2 101,62 + 2 080,27 ] /2 = 2
090,94 cm–1
Énergie (raie
manquante) = [ 2 098,59 + 2 077,31 ] /2 = 2
087,95 cm–1
Les vraies valeurs, plus rigoureuses, vont
apparaître lors de la résolution de la
cubique E = ¦(m),
après avoir changé la variable J en
m. Il est donc nécessaire d'établir
pour chaque raie, sa valeur de J. Les deux
séries de raies se présentent sous la forme
de deux lobes, l'un plus riche en énergie que
l'autre. On identifiera ainsi les raies riches et les
raies pauvres dans chacun des cas. La raie la moins
énergétique de la bande riche porte la
valeur de J = 0 et la raie la plus
énergétique de la bande pauvre porte la
valeur J = 1. On peut donc remplir les
colonnes 3 et 7 du tableau.
|
nº
|
Énergie
(cm–1)
|
JD35Cl
|
m
|
nº
|
Énergie
(cm–1)
|
JD37Cl
|
m
|
|
1
|
2230,8479
|
+ 15
|
+ 16
|
|
|
|
|
|
2
|
2224,0387
|
+ 14
|
+ 15
|
|
|
|
|
|
3
|
2216,9606
|
+ 13
|
+ 14
|
4
|
2213,6323
|
+ 13
|
+ 14
|
|
5
|
2209,6132
|
+ 12
|
+ 13
|
6
|
2206,3007
|
+ 12
|
+ 13
|
|
7
|
2202,0025
|
+ 11
|
+ 12
|
8
|
2198,7071
|
+ 11
|
+ 12
|
|
9
|
2194,1272
|
+ 10
|
+ 11
|
10
|
2190,8502
|
+ 10
|
+ 11
|
|
11
|
2185,9952
|
+ 9
|
+ 10
|
12
|
2182,7377
|
+ 9
|
+ 10
|
|
13
|
2177,6036
|
+ 8
|
+ 9
|
14
|
2174,3672
|
+ 8
|
+ 9
|
|
15
|
2168,9620
|
+ 7
|
+ 8
|
16
|
2165,7472
|
+ 7
|
+ 8
|
|
17
|
2160,0666
|
+ 6
|
+ 7
|
18
|
2156,8750
|
+ 6
|
+ 7
|
|
19
|
2150,9268
|
+ 5
|
+ 6
|
20
|
2147,7596
|
+ 5
|
+ 6
|
|
21
|
2141,5397
|
+ 4
|
+ 5
|
22
|
2138,3978
|
+ 4
|
+5
|
|
23
|
2131,9144
|
+ 3
|
+ 4
|
24
|
2128,7986
|
+ 3
|
+ 4
|
|
25
|
2122,0484
|
+ 2
|
+ 3
|
26
|
2118,9605
|
+ 2
|
+ 3
|
|
27
|
2111,9499
|
+ 1
|
+ 2
|
28
|
2108,8904
|
+ 1
|
+ 2
|
|
29
|
2101,6186
|
0
|
+ 1
|
30
|
2098,5888
|
0
|
+ 1
|
|
|
raie manquante
|
|
|
|
raie manquante
|
|
|
|
31
|
2080,2753
|
+ 1
|
- 1
|
32
|
2077,3076
|
+ 1
|
- 1
|
|
33
|
2069,2694
|
+ 2
|
- 2
|
34
|
2066,3342
|
+ 2
|
- 2
|
|
35
|
2058,0468
|
+ 3
|
- 3
|
36
|
2055,1451
|
+ 3
|
- 3
|
|
37
|
2046,6072
|
+ 4
|
- 4
|
38
|
2043,7399
|
+ 4
|
- 4
|
|
39
|
2034,9590
|
+ 5
|
- 5
|
40
|
2032,1271
|
+ 5
|
- 5
|
|
41
|
2023,1001
|
+ 6
|
- 6
|
42
|
2020,3044
|
+ 6
|
- 6
|
|
43
|
2011,0405
|
+ 7
|
- 7
|
44
|
2008,2814
|
+ 7
|
- 7
|
|
45
|
1998,7764
|
+ 8
|
- 8
|
46
|
1996,0555
|
+ 8
|
- 8
|
|
47
|
1986,3186
|
+ 9
|
- 9
|
48
|
1983,6365
|
+ 9
|
- 9
|
|
49
|
1973,6637
|
+ 10
|
- 10
|
50
|
1971,0211
|
+ 10
|
- 10
|
|
51
|
1960,8216
|
+ 11
|
- 11
|
52
|
1958,2191
|
+ 11
|
- 11
|
|
53
|
1947,7905
|
+ 12
|
- 12
|
54
|
1945,2297
|
+ 12
|
- 12
|
|
55
|
1934,5784
|
+ 13
|
- 13
|
56
|
1932,0590
|
+ 13
|
- 13
|
|
57
|
1921,1853
|
+ 14
|
- 14
|
58
|
1918,7094
|
+ 14
|
- 14
|
|
59
|
1907,6167
|
+ 15
|
- 15
|
|
|
|
|
|
60
|
1893,8780
|
+ 16
|
- 16
|
|
|
|
|
On peut essayer de porter sur un graphe
les valeurs des énergies de chacune des raies en
fonction de J (figure 1). On voit que ces
courbes ne permettent pas d'obtenir la valeur de
l'énergie de la transition vibrationnelle pure en
utilisant l'ensemble des données
numériques.
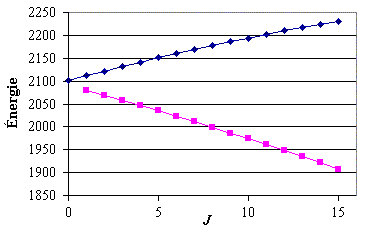
Figure 1. Variation de l'énergie des raies en
fonction de J (cas
D35Cl).
Après avoir identifié les
valeurs de J, il convient d'effectuer les
changements de variables appropriés. Pour les
raies riches, le changement de variables est tel que
m = J + 1 et pour les
raies pauvres, m = –J. On
constitue ainsi les 4e et 8e
colonnes du tableau précédent. Pour
compléter les calculs, il ne reste plus
qu'à effectuer une régression d'ordre 3 en
m sur chacune des deux molécules.
ΔE
= b + am +
cm2 + dm3
Dans cette équation :
- l'ordonnée à l'origine b est
l'énergie de la transition vibrationnelle pure,
égale à ωe –
2 ωexe;
- a = B″ + B′,
où B″ et B′ sont les constantes
rotationnelles dans chacun des deux niveaux de
vibration;
- c = B″ – B′;
- d = – 4 D, où D
est la constante de distorsion centrifuge.
L'utilisation d'un chiffrier, ou encore
d'un logiciel graphique ou statistique, établit
les deux relations suivantes :
Figure 2 : y
(D35Cl) = –0,0006
m3 – 0,1121 m2
+ 10,6719m + 2091,0506
R 2 = 1,0000
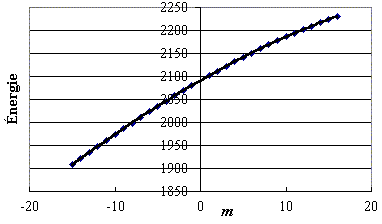
Figure 2. Énergie des raies en fonction de
m (cas
D35Cl).
Figure 3 : y
(D37Cl) = –0,0006
m3– 0,1117 m2 +
10,6409 m + 2088,0547
R 2 = 1,0000
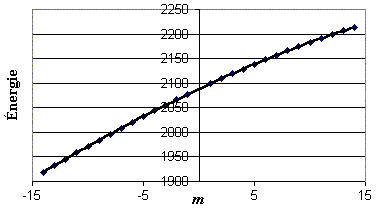
Figure 3. Énergie des raies en fonction de
m (cas
D37Cl).
On obtient donc les valeurs
suivantes :
|
Molécule
|
ωe –
2 ωexe
(cm–1)
|
B′
(cm–1)
|
B″
(cm–1)
|
D
(cm–1)
|
|
D35Cl
|
2091,0516
|
5,3918
|
5,2797
|
1,5 10–4
|
|
D37Cl
|
2088,4893
|
5,3763
|
5,2646
|
1,5 10–4
|
On notera que les valeurs de ωe
sont significativement différentes des moyennes
arithmétiques calculées en début de
problème.
-
Réponses :
B′ (D35Cl,
υ = 0) = 5,3922 cm–1;
B″ (D35Cl, υ =
2) = 5,1684 cm–1.
-
La relation qui existe entre la constante
de rotation et le niveau de vibration est :
Bυ
= Be – αe
(υ + 1/2) + ...
On peut dès lors compléter
le tableau qui suit et noter la bonne coïncidence
entre les résultats théoriques et ceux
obtenus précédemment.
|
υ
|
B (cm–1)
|
|
théorique
|
problèmes 6 et 7
|
|
0
|
5,392 215
|
5,392 2
|
|
1
|
5,278 857
|
5,2797
|
|
2
|
5,165 566
|
5,168 4
|
-
Si I est le moment d'inertie, μ
la masse réduite et r la longueur de la
liaison, alors la constante de rotation B est
donnée par :
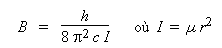
La constante de rotation d'une
molécule diatomique varie comme l'inverse de la
distance internucléaire au carré. Donc sur
un graphe, si l'on porte la grandeur B en fonction
de l'inverse de cette distance au carré on doit
obtenir une droite. C'est ce que montre le graphe qui
suit. Notons que le coefficient de corrélation
R 2 est bien égal à
l'unité.
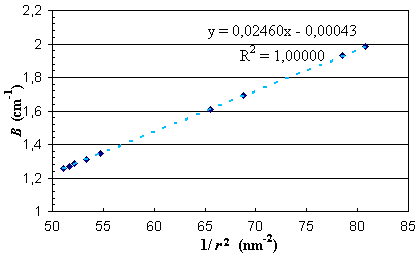
Figure 4. Variations de B
en fonction de l'inverse du carré de la longueur
de la liaison C=O.
Par ailleurs, le module n'apporte pas de
réponse quant à une éventuelle
dépendance de ωe en
fonction de la longueur de la liaison. Le tableau des
données indiqué plus haut montre que ωe
diminue avec l'allongement de la liaison. Cela est
confirmé par le graphe qui suit. Cette figure ne
précise évidemment pas le type de relation
entre les deux grandeurs.
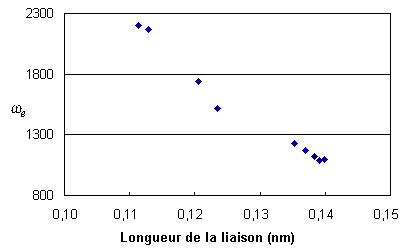
L'obtention d'une courbe de tendance peut
parfois aider à préciser cette
dépendance. Une régression linéaire
et une régression polynomiale d'ordre 2 donnent
les équations suivantes :
y = – 3854,1
x + 6 439,8 avec R 2 =
0,9762
y = – 8398,7
x2 – 25040 x + 19 693
avec R2 = 0,9945
Le coefficient de corrélation donne
un avantage à la dépendance quadratique de
ωe sur la longueur de la liaison.
La différence, pour significative qu'elle soit,
n'est pas suffisante pour confirmer cette
dépendance.
-
Ce problème est simple à
solutionner. Il s'agit seulement de traduire en chiffres
la relation suivante :
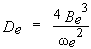
D'où :
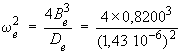
ωe2
= 1,542 × 106
(cm–1)2
et ωe
= 1 240 cm–1
La valeur ainsi calculée est
inférieure à la valeur observée qui
est de 1 285,08 cm–1, soit un
écart d’environ 3,5 %.
Corrigés des problèmes
avec VR Molécules
-
Les constantes apparaissent dans
l'expression du terme spectral, où la constante
rotationnelle B inclut la correction due à
l'interaction vibration-rotation :
E(υ,
J) = G(υ)
+ F(J)
E(υ,
J) = ωe (υ
+ 1/2) – ωexe (υ
+ 1/2)2 +
[ Be – αe (υ
+ 1/2) ] J (J + 1)
Pour un maximum de précision, on
emploiera les plus grandes valeurs possibles des nombres
quantiques.
Pour ωe, on
utilise l'énergie du niveau υ = 5,
avec J = 0 et l'anharmonicité
désactivée. On trouve :
ωe = 16 450 / 5,5 = 2 990,9 cm–1
Pour ωexe,
on évalue, toujours pour le niveau υ
= 5, la différence d'énergie ΔE
avec et sans l'anharmonicité, égale
à ωexe (υ
+ 1/2)2. On trouve :
ωexe = ΔE (υ,
J) / (υ +
1/2)2 = (16 450 – 14 850)
/ 5,52 = 53 cm–1.
Be est
déterminé à partir de
l'énergie pour J = 30 :
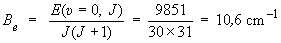
Finalement, αe est
déterminé à partir de la
différence d'énergie ΔE, pour
υ = 5 et
J = 30, avec et sans interaction
vibration-rotation, égale à :
αe (υ
+ 1/2) J (J + 1)
On trouve :
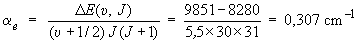
-
Les masses réduites de
H2 et HD sont respectivement égales
à 1/2 et 2/3. Le rapport μ / μi
est donc égal à 3/4.
Le rapport
Be,i / Be
est égal à 42 500 / 56
540 = 0,752, ce qui est conforme
à l'équation 3.7.
Le rapport ωe,i / ωe
est égal à 20 970 /
24 170 = 0,868, une valeur
proche de la racine carrée de μ / μi
(0,866), prédite par
l'équation 3.8.
Le rapport ωe,ixe,i / ωexe
est égal à (20 970 – 18 190)
/ (24 170 – 20 500) = 0,757,
ce qui est conforme à
l'équation 3.9.
-
Employez la même méthode
qu'au problème VR Molécules nº 1,
et vérifiez vos réponses dans le
WebBook du site du NIST : http://webbook.nist.gov/chemistry/name-ser.html.
Note : Les constantes correspondant à la
molécule dans son état électronique
fondamental sont à la dernière ligne des
tableaux.
|



