|
|
MODULE 1 Rotation des
molécules diatomiques
Problèmes
- Calculez, en cm–1, la position
(l'énergie) des quatre premières raies
purement rotationnelles pour la molécule ClF
(rCl–F = 163 pm),
ainsi que la constante de distorsion centrifuge
D = 0,5 × 10–4 B.
On prendra 35 comme valeur pour la masse de l'atome de
chlore. Corrigé
-
La molécule HF a des raies
rotationnelles séparées de
41,9 cm–1. Calculez son moment
d'inertie, la longueur de la liaison et sa vitesse
angulaire dans les quatre premiers niveaux rotationnels.
Corrigé
-
Si la longueur de la liaison H-Cl
était multipliée par 10, sans
altération de la masse de la molécule, le
spectre d'absorption rotationnel serait-il
altéré? Si oui, comment? Corrigé
-
La distance N–0 dans la
molécule d'oxyde nitrique est de 115 pm.
- Calculez son moment d'inertie dans les
systèmes C.G.S. et SI.
- Calculez l'énergie pour les niveaux de
rotation J = 1, 2, 3, 4 :
- En ergs/molécule;
- En cal/mole;
- En joules/mole.
- Calculez, en nombre d'ondes, la fréquence
de la raie d'absorption lorsque J passe de
0 → 1, 1 → 2 et 2 → 3.
Corrigé
-
La constante rotationnelle B dans
H35Cl est de 10,34 cm–1;
calculez la valeur de la même constante dans
H37Cl. Corrigé
-
A. Honig et autres [Phys. Rev.,
96, 629 (1954)] ont étudié les
spectres de rotation des halogénures alcalins. Le
tableau suivant donne les valeurs qu'ils ont obtenues
pour les transitions J = 8 → 9
entre les niveaux de rotation du bromure du rubidium
gazeux, au niveau fondamental de vibration (υ = 0) :
|
Molécule
|
ν × 10–6
(s–1)
|
|
85Rb79Br
|
25 596,03 ± 0,10
|
|
87Rb79Br
|
25 312,99 ± 0,10
|
|
85Rb81Br
|
25 268,84 ± 0,10
|
où ν désigne
la fréquence de la transition.
En supposant que la molécule RbBr se comporte
comme un rotateur rigide, calculez, d'après les
valeurs données ci-dessus, les distances
internucléaires des molécules isotopes de
RbBr, les masses atomiques des différents isotopes
étant les suivants [T. L. Collins et autres,
Phys.Rev., 94, 398 (1954)].
79Br : 78,943
65
85Rb : 84,939 20
81Br : 80,942
32
87Rb : 86,937 09.
Corrigé
-
Dans la série des composés
diatomiques 1H–X proposés dans le
tableau suivant, montrez théoriquement, en
négligeant la masse de l'atome d'hydrogène
devant celle de l'atome X, que la valeur de B est
une fonction de
1 / re2.
Vérifiez expérimentalement le
résultat en traçant le graphe
approprié. Corrigé
|
Molécule
|
État fondamental
|
B (cm–1)
|
re (nm)
|
|
1H–14N
|
X 3Σ–
|
16,699
|
0,103 62
|
|
1H–16O
|
X 2Πi
|
18,911
|
0,096 97
|
|
1H–19F
|
X 1Σ+
|
20,956
|
0,091 68
|
|
1H–24Mg
|
X 2Σ+
|
5,8257
|
0,172 97
|
|
1H–32S
|
X 2Πi
|
9,46
|
0,1341
|
|
1H–35Cl
|
X 1Σ+
|
10,593
|
0,1274
|
|
1H–40Ca
|
X 2Σ+
|
4,277
|
0,200 25
|
|
1H–58Ni
|
X 2Δ
|
7,700
|
0,147 56
|
|
1H–64Zn
|
X 2Σ+
|
6,679
|
0,159 49
|
|
1H–81Br
|
X 1Σ+
|
8,465
|
0,141 44
|
|
1H–115In
|
X 1Σ+
|
4,994
|
0,1838
|
|
1H–138Ba
|
X 2Σ+
|
3,3828
|
0,223 17
|
|
1H–174Yb
|
X 2Σ+
|
3,9930
|
0,2053
|
|
1H–205Tl
|
X 1Σ+
|
4,806
|
0,1870
|
|
Valeurs
tirées de Huber, K. P. et
G. Herzberg, Molecular Spectra and
Molecular Structure IV. Constants of Diatomic
Molecules, Van Nostrand Reinhold Co., New
York, 1979.
|
Problèmes avec VR
Molécules
-
Placez VR Molécules à la
page 3â.
Notez dans un tableau semblable à celui qui
apparaît ci-dessous les valeurs de l'énergie
pour les 6 premières valeurs non nulles du nombre
quantique J
|
J
|
0
|
1
|
2
|
3
|
4
|
5
|
6
|
|
E (cm–1)
|
0
|
|
|
|
|
|
|
|
ΔE
|
–
|
|
|
|
|
|
|
|
Δ(ΔE)
|
–
|
|
|
|
|
|
|
L’énergie augmente-t-elle de
manière proportionnelle aux valeurs de
J ?
Allez plus loin dans le traitement des données et
calculez les différences d’énergie
entre les valeurs successives de J. Ces valeurs
sont-elles proportionnelles aux valeurs
de J ?
Finalement, calculez les deuxièmes
différences, Δ(ΔE) = ΔE(J) – ΔE(J–1).
Que concluez-vous? Corrigé
-
Placez VR Molécules à la
page 2.
En observant attentivement les mouvements des deux
molécules, ou encore en utilisant la petite
horloge en bas à droite de VR Molécules,
essayez de chiffrer approximativement le rapport des
vitesses de rotation de ces molécules, pour un
même nombre quantique. Déterminez
également le rapport des énergies des deux
molécules.
Comment ces rapports se comparent-ils avec celui des
masses réduites?
Corrigé
-
Placez VR Molécules à la
page 5,
qui présente (en deux exemplaires) la
molécule DCl, soit une molécule HCl
où l'hydrogène a été
remplacé par son isotope de masse 2, le
deutérium. Celui-ci possède un neutron
excédentaire, représenté par le
point noir au centre de l'atome.
En faisant varier l'énergie de rotation et en
activant si nécessaire la correction
d'énergie appropriée, déterminez les
valeurs des constantes D et B pour cette
molécule. Corrigé
-
Placez VR Molécules à la
page 6,
qui présente la molécule
d'hydrogène. Activez la correction liée
à la distorsion centrifuge et examinez comment
varie l'énergie en fonction du nombre quantique
J. Remarquez-vous quelque chose
d'étrange?
Le phénomène en question provient des
limites du modèle utilisé pour la
simulation VR Molécules, qui inclut, si on
l'active bien sûr, le terme de correction pour
distorsion centrifuge décrit dans le module.
Cependant, celui-ci n'est que le premier terme d'une
série de corrections faisant intervenir les
puissances de J (J+1).
Les deux premiers termes de cette série
s'écrivent :
ΔEcentrifuge
(J) = – DJ 2 (J+1)2 + HJ 3 (J+1)3
Le terme contenant le facteur H,
beaucoup plus petit que D, entraîne
généralement une correction
négligeable... sauf, visiblement, pour
l'hydrogène. Cette molécule est celle qui
possède le moment d'inertie le plus faible; elle
présente donc les constantes de rotation les plus
importantes. La prise en compte du terme cubique devient
nécessaire, aux valeurs de J
élevées, pour contrer la valeur excessive
du terme quadratique.
À partir de ce que vous avez constaté en
observant le comportement étrange du
modèle, pouvez-vous estimer l'ordre de grandeur de
la constante H pour la molécule
d'hydrogène? Corrigé
Corrigés
-
Les raies rotationnelles correspondent aux
transitions effectuées par la molécule
entre ses niveaux de rotation. Il est donc
nécessaire de calculer l’énergie de
ces niveaux de rotation, F(J), puis de
calculer les différences d'énergie entre
ces niveaux pour obtenir les énergies des
transitions. Les valeurs de F(J) sont
reliées aux valeurs de la constante rotationnelle
B et de la constante de distorsion centrifuge
D de la molécule à travers la
relation :
F(J) = BJ (J
+1) – DJ
2 (J +1)
La valeur relative des deux constantes est
indiquée, il suffit donc de calculer la valeur de
la constante B. Cette constante rotationnelle est
reliée au moment d’inertie de la
molécule :
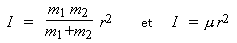
puisque μ est la masse
réduite. En se rappelant que les masses des atomes
de chlore et de fluor sont respectivement de 35,5 et de
19 g/mole, calculons la valeur de I dans le
système SI :
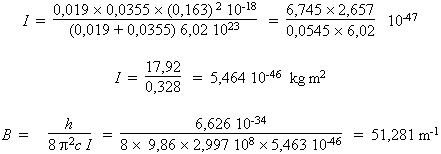
B = 0,513
cm–1
On peut dès maintenant
établir l'énergie de chacun des niveaux
J; en remplaçant B et D par
leur valeurs, on obtient :
|
J
|
F(J)
|
Énergie (cm–1)
|
|
0
|
0
|
0
|
|
1
|
2 B – 4 D
|
1,026 –
3,5 × 10–6
= 1,026
|
|
2
|
6 B – 36D
|
3,078 – 3,157 10–5
= 3,078
|
|
3
|
12 B – 144 D
|
6,156 –
1,26 × 10–4
= 6,156
|
|
4
|
20 B – 400 D
|
10,26 –
3,51 × 10–4
= 10,26
|
Ces calculs montrent que la correction
pour la distorsion centrifuge est ici négligeable.
Les transitions rotationnelles doivent obéir
à la règle de sélection, ΔJ = ±1.
En absorption, on aura donc comme transition les quatre
transitions suivantes (ΔJ = +1) :
|
J + 1 ← J
|
Énergie (cm–1)
|
|
1 ← 0
|
1,026
– 0 = 1,026
|
|
2 ← 1
|
3,078 – 1,026 =
2,053
|
|
3 ← 2
|
6,156 – 3,078
= 3,078
|
|
4 ← 3
|
10,26 – 6,156 =
4,10
|
-
- Dans un spectre de rotation, la
séparation observée entre deux raies
consécutives est égale à deux
fois la constante de rotation :
2B = 41,9 cm–1.
Cette constante est elle-même liée au
moment d’inertie de la molécule. Dans le
système d'unités SI, on obtient :
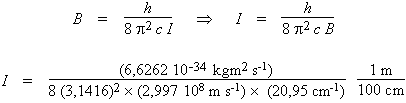
I = 1,336 × 10–47
kg · m2
- Le moment d’inertie est relié à
la distance internucléaire à travers la
relation I = μr2
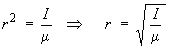
μ est la masse
réduite du rotateur :
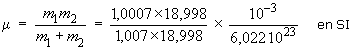
μ
= 1,587 10–27 kg
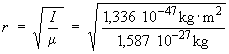
⇒ r =
0,917 10–10 m = 91,7
pm
- Le moment cinétique, P, peut
s'écrire : P = Iωoù
ω est la vitesse angulaire du rotateur.
On peut donc écrire :
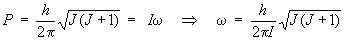
Donc :
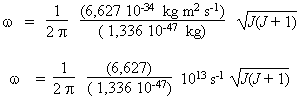
On peut maintenant compléter le
tableau de résultats qui suit :
|
J
|
[ J(J+1) ]1/2
|
ω ( s–1)
|
|
0
|
0
|
0
|
|
1
|
21/2
|
1,116 × 1013
|
|
2
|
61/2
|
1,934 × 1013
|
|
3
|
121/2
|
2,735 × 1013
|
-
On a vu que les raies d'absorption qui
correspondent aux transitions rotationnelles sont
espacées d'une distance (énergie
exprimée en cm–1) égale
à 2 fois la valeur de la constante rotationnelle
B (en ignorant l'effet de la distorsion
centrifuge). En se rappelant les formules reliant cette
constante B, le moment d'inertie I et la
longueur de la liaison r, on trouve :
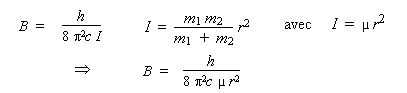
Si la valeur de r est
multipliée par un facteur 10, la valeur de
B est divisée par un facteur 100. L'espace,
l'énergie entre deux raies, est donc divisé
par le même facteur 100. Le spectre de rotation
serait donc fortement affecté. Tout se passerait
comme si ce spectre était compressé d'un
facteur 100.
-
- Le problème revient à
employer les formules utilisées
précédemment :
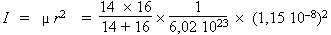
I = 1,64 10
–39 g · cm2
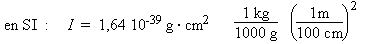
I = 1,64 × 10–46
kg · m2
- Le moment d'inertie venant d'être
calculé, on peut calculer la valeur de la
constante rotationnelle :
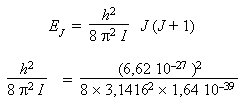
E =
3,38 × 10–16
ergs
E = 3,38 × 10–23
joules
On peut maintenant, en
répétant les calculs pour
différentes valeur de J,
compléter le tableau suivant :
|
J
|
J (J + 1)
|
EJ
(ergs/molécule)
|
EJ
(ergs/mole)
|
EJ
(J/mol)
|
|
1
|
2
|
6,76 × 10–16
|
40,8 × 107
|
40,8
|
|
2
|
6
|
20,34 × 10–16
|
122,4 × 107
|
122,4
|
|
3
|
12
|
40,68 × 10–16
|
244,8 × 107
|
244,8
|
|
4
|
20
|
67,78 × 10–16
|
408 × 107
|
408
|
- L'énergie de la transition entre deux
niveaux est évidemment égale à la
différence d'énergie entre ces niveaux.
Par exemple :
E2 – E1 = 122,4 – 40,8 = 81,6
J/mol.
Pour exprimer cette énergie en
nombre d'ondes, il faut se rappeler que  = E/hc,
où E est l'énergie d'un photon,
donc l'énergie perdue par une seule
molécule. On obtient ainsi : = E/hc,
où E est l'énergie d'un photon,
donc l'énergie perdue par une seule
molécule. On obtient ainsi :
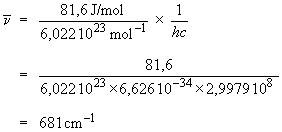
-
On peut raisonnablement penser que la
longueur de la liaison r (H–37Cl)
est identique à r (H–35Cl).
Le moment d'inertie est
I = μr2. Par
ailleurs, la constante de rotation B est telle
que :
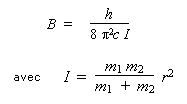
La solution du problème peut
être obtenue en calculant pour chacune des deux
molécules isotopiques sa valeur de B.
Comme la longueur de la liaison n'est pas
indiquée, on obtiendra les valeurs de
B35 et de B37 avec un
paramètre r. En faisant le rapport des
deux valeurs de B ainsi obtenues, le
paramètre r disparaîtra, et de la
valeur de la constante B35, on
obtiendra la valeur de la constante
B37. Cette méthode exige de
faire deux fois le même calcul. Cela n'est pas
nécessaire et peut donc être
évité en réécrivant la
formule précédente. En posant
m1 la masse de l'atome
d'hydrogène et m2 la masse de
l'atome de chlore, on peut en effet
écrire :
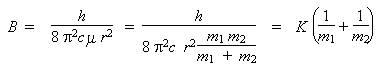
K est une constante de
proportionnalité. Donc,

D'où
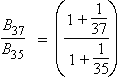
ou encore, en utilisant la loi des
proportions :
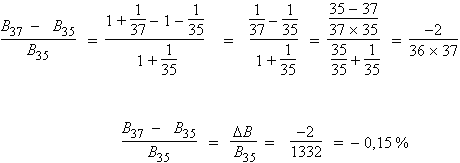
B37 –
B35 = ΔB =
10,34 × 0,15 % = 0,0155
cm–1
et
B37 = 10,34 –
0,0155 = 10,325 cm–1
-
L'énergie d'un niveau quelconque
d'un rotateur rigide (pas de distorsion centrifuge, ou
encore D = 0) est donnée par la
relation :
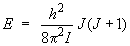
Le niveau J = 8 a donc
une énergie telle que :
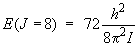
et l'énergie du niveau
J = 9 est telle que :
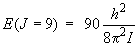
La différence d'énergie
entre les deux niveaux est donc égale
à :
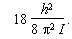
L'énergie de la transition est
donc :
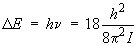
D'où :
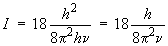
De cette relation, connaissant la
fréquence de la transition et la constante de
Planck, on obtient la valeur de I dans chacun des
cas. Le calcul est exprimé avec les unités
SI.
- 85Rb79Br
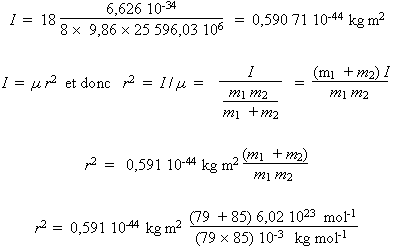
r2 = 0,868
50 × 10–19 m
2
r = 247
pm
- 87Rb79Br
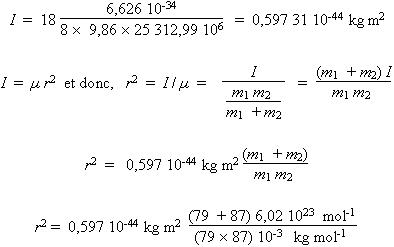
r2 = 0,868
47 × 10–19
m2
r = 247
pm
- 85Rb81Br
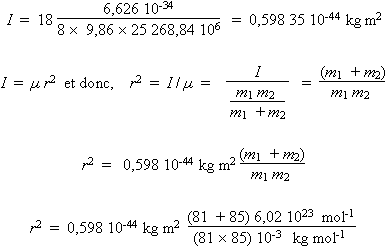
r2 =
0,858 72 × 10–19
m2
r = 293
pm
-
On sait que la constante rotationnelle est
telle que
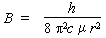
B est donc bien une fonction de
1 /μr2 où μ,
la masse réduite, est telle que :
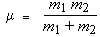
On constate que la valeur de la masse
réduite est presque constante, variant entre 0,93
et 0,995 pour l'ensemble des molécules du tableau;
on peut donc considérer que B est une
fonction de 1 / r2
seulement.
La solution du problème est
relativement simple. En utilisant un chiffrier comme
Excel on obtient le tableau de valeurs et le graphe qui
suivent montrant la variation de B en fonction de
1 / r2.
|
Molécule
|
B (cm–1)
|
re (nm)
|
1 / r2
|
|
1H–14N
|
16,699
|
0,103 62
|
93,13
|
|
1H–16O
|
18,911
|
0,096 97
|
106,3
|
|
1H–19F
|
20,956
|
0,091 68
|
118,9
|
|
1H–24Mg
|
5,8257
|
0,172 97
|
033,4
|
|
1H–32S
|
9,46
|
0,1341
|
55,6
|
|
1H–35Cl
|
10,59
|
0,1274
|
61,6
|
|
1H–40Ca
|
4,277
|
0,200 25
|
25,0
|
|
1H–58Ni
|
7,700
|
0,147 56
|
45,9
|
|
1H–64Zn
|
6,679
|
0,159 49
|
39,3
|
|
1H–81Br
|
8,465
|
0,141 44
|
50,0
|
|
1H–115In
|
4,994
|
0,1838
|
29,6
|
|
1H–138Ba
|
3,3828
|
0,223 17
|
20,1
|
|
1H–174Yb
|
3,9930
|
0,2053
|
23,7
|
|
1H–205Tl
|
4,806
|
0,1870
|
28,6
|
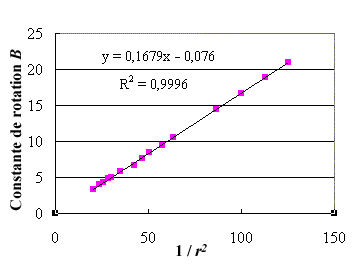
L'équation de la droite B =
f (1/r2) est :
y = –0,0761
+ 0,16788 x avec R 2
= 9,9996
où y est exprimé en
cm–1 et x
en nm–2.
La pente de cette droite, notée
b, qui a pour unités des cm–1
nm2, est reliée au rapport
h/c :
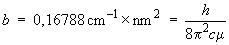
On peut donc calculer (c'est-à-dire
obtenir expérimentalement) le rapport
h/c.
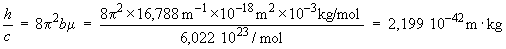
ce qui est très proche de la valeur
directement calculée à partir des valeurs
admises des constantes h et c, soit 2,210
921 10–42 m · kg.
Corrigés des problèmes
avec VR Molécules
|
J
|
0
|
1
|
2
|
3
|
4
|
5
|
6
|
|
E(cm–1)
|
0
|
20,88
|
62,64
|
125,3
|
208,8
|
313,2
|
438,5
|
|
ΔE
|
–
|
20,88
|
41,76
|
62,9
|
83,5
|
104,4
|
125,3
|
|
Δ(ΔE)
|
–
|
20,88
|
20,88
|
21,1
|
20,6
|
20,9
|
21,1
|
On remarque que les valeurs de
l'énergie (première ligne de données
du tableau) n'augmentent pas proportionnellement au
nombre J; c'est le cas cependant pour les
différences ΔE. Finalement, on
constate que les deuxièmes différences, Δ(ΔE),
sont constantes (dans la mesure permise par le nombre de
chiffres significatifs). Comme ΔE
représente la fréquence de la transition
entre deux niveaux de rotation voisins, on en conclut que
les fréquences de transition successives du
spectre de rotation seront également
espacées.
-
On peut mesurer les valeurs suivantes pour
J = 25 :
HCl : 10 tours en 0,44 ps environ, soit 23
tours/ps, ou
2,3 × 1013 tours/seconde;
O2: 1 tour en 0,33 ps environ, soit
3,0 tours/ps, ou
3,0 × 1013 tours/seconde.
Le rapport entre les vitesses de rotation de HCl et de
O2 est donc d'environ 7,7.
Par ailleurs, le rapport des énergies, soit
E(HCl) / E(O2), est
égal à
6786 / 929,5 = 7,3.
Ces deux rapports sont proches de l'inverse du rapport
des masses réduites des molécules, soit μ(O2) / μ(HCl) = 8 / 1,03 = 7,8.
Ces résultats s'expliquent par le fait que la
distance entre les atomes est sensiblement la même
dans les deux molécules.
-
En l'absence de distorsion centrifuge,
l'énergie du niveau J est donnée en
unités de nombre d'ondes par :
F(J) = BJ
(J+1)
La valeur de B peut donc être
déterminée à partir de celle de
l'énergie pour un niveau J quelconque. Pour
un maximum de précision, prenons le niveau
J = 30; on trouve alors :
B = F(30) / (30×31) = 5015
/ 930 = 5,39 cm–1
Pour déterminer la valeur de la
constante D, il faut activer la correction de
distorsion centrifuge pour la molécule de gauche.
Si la valeur de la constante B est connue, une
seule valeur d'énergie est alors requise pour
déterminer la valeur de D.
D'après l'équation 1.11, on a en
effet :
DJ 2
(J+1)2 = BJ
(J+1) – F(J)
où F(J) est la valeur
incluant la correction et BJ (J+1) la
valeur sans correction. On obtient, toujours en
considérant J = 30 :
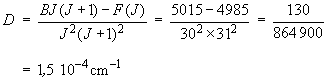
-
L'énergie de rotation, au lieu
d'augmenter constamment avec le nombre J, atteint
une valeur maximum d'environ 19 000 cm–1
à J = 25, pour diminuer par la
suite. La correction pour distorsion centrifuge, qui
inclut uniquement le premier terme, est donc trop grande;
à J = 30, elle réduit
l'énergie de 55 000 à
15 000 cm–1.
On peut estimer l'ordre de grandeur de la
constante H si l'on fait l'hypothèse que le
terme qui lui est associé devrait ramener la
valeur de l'énergie à une valeur beaucoup
plus proche de la valeur non corrigée. On
supposera qu'à J = 30 cette
valeur serait de l'ordre de 50 000 cm–1.
On pourrait supposer une valeur différente, par
exemple 40 000 cm–1, mais
comme on cherche un ordre de grandeur, cela ne changerait
pas vraiment le résultat.
Le second terme de correction devrait donc
ajouter à la valeur corrigée au premier
ordre environ 35 000 cm–1, ce
qui permet d'écrire :
H ≈ 35 000
/ J 3
(J+1)3 = 35 000
/
(8 × 108) ≈ 4 × 10–5 cm–1
Notons que la valeur réelle de
cette constante est 4,7 × 10–5 cm–1.
|



